170号 AUTUMN 目次を見る
キーワード:歯周治療とEr:YAGレーザー/非外科的術式「Er-LCPT」
■目 次
- ≫ はじめに
- ≫ 1. 優れた原因除去で炎症をコントロール
- ≫ 2. Er:YAGレーザースケーリングの実際
- ≫ 3. 新しい非外科的術式「Er-LCPT」
- ≫ 4. 低侵襲の歯周外科への応用―マイクロサージェリーとのコンビネーション―
- ≫ 5. 治癒と組織再生を促進するメカニズム
- ≫ まとめ
■はじめに
現在、歯科用Er:YAGレーザーは国内で累計販売実績として5,000台以上となっており、近年は日常診療に取り入れているクリニック数も毎年、上昇傾向にある。これは、う蝕治療や歯周治療などの一般歯科臨床におけるEr:YAGレーザーの有効性の高さや、それに対応した項目の保険収載などを反映していると考えられる。
本稿では、歯周治療においてEr:YAGレーザーを効果的に活用するための基礎知識を症例とあわせて紹介する。
■1. 優れた原因除去で炎症をコントロール
歯周治療では炎症の原因であるプラークとその主な増悪因子である歯肉縁下歯石を確実に除去しなければならない。また、歯周ポケット内の炎症性結合組織(肉芽組織)には、歯周病原菌の侵入や、組織破壊を促す細胞伝達物質(サイトカイン)の過度な発現がみられる。
Er:YAGレーザーの波長2,940nmは、軟組織と硬組織の両者を熱傷害なく蒸散できるため、歯石、細菌、菌体外毒素だけでなく炎症性結合組織の除去も一括でできる。これがEr:YAGレーザーを歯周治療に用いるうえでの最大の強みとなっている。
歯石には、水分や有機成分が多く含まれる。それらに吸収された光エネルギーは、熱エネルギーに変換されて水蒸気を生じ、微小爆発が起こることで、歯石が熱傷害なく蒸散される(図1)。
1994年にAokiらがEr:YAGレーザーによる歯石除去の詳細を世界で初めて報告し1)、歯石の除去は歯の長軸方向に斜め20~30度ほどで歯根面に接触型のチップを沿わせながら、注水冷却を併用して歯石の側面から蒸散する方法2)が推奨されている(図2)。
この方法は、歯質を保存しつつ効率的に歯石を蒸散させることができる。さらに、切削片によるチップ先端の汚染や損傷は蒸散効率の低下に直結するため3)、斜めからの注水照射はそれらを防ぐという利点もある。
Er:YAG レーザーはチップ接触部で歯石蒸散をできるだけでなく、散乱した照射光が及ぶ範囲全体が殺菌や無毒化の対象になっていると考えられている。これは、通常用いる出力の1/20~1/100程度の非常に低い出力で、高い殺菌効果5、6)や細菌由来の内毒素(リポ多糖)除去効果が期待できる7)ためであり、臨床的な利点となっている。その結果、Er:YAGレーザーによるデブライドメントは、生体にとって親和性のある根面を包括的に形成できると推測される(図3)。
日本歯周病学会と日本レーザー歯学会から歯石除去について共同の学会見解論文4)が両学会のホームページで公開されており、参照されたい。
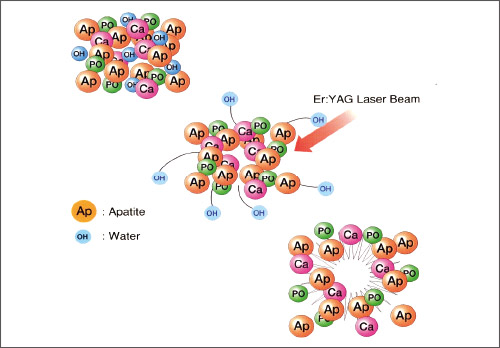
図1 Er:YAGレーザーの硬組織蒸散モデル。Er:YAGレーザーの波長は硬組織や歯石中の水分を一気に水蒸気化し、熱傷害なく切削が可能となる。-
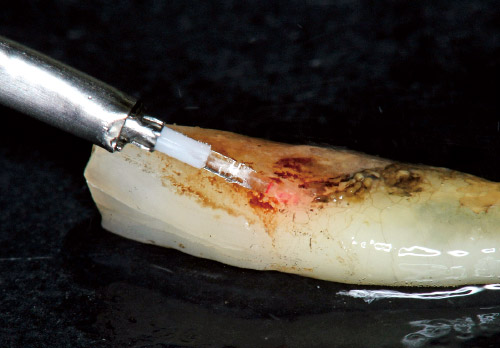
図2 斜め照射での歯石除去。コンタクトチップを根面に対して20~30度の角度で、歯冠側方向から注水下で照射すると、健全歯質を保存し、チップの損傷が少なく、蒸散ができる。 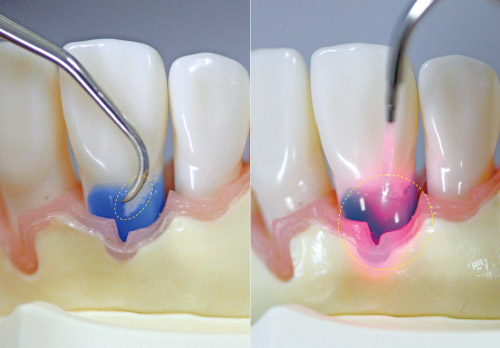
図3 器具が触れた部分しか作用が生じない機械的処置と異なり、レーザーは光がチップ周辺に拡散し、この弱い低出力の光で殺菌、無毒化、生体刺激の効果が期待できる。
■2. Er:YAGレーザースケーリングの実際
これまで、Er:YAGレーザーをスケーリング・ルートプレーニング(SRP)に応用した臨床研究は多く報告されている。Schwarzらは手用器具と比較して処置時間は短く、プロービング時の出血(BOP)およびアタッチメントレベルにおいてレーザー群のほうが有意に高い改善であったと報告している8)。
【症例1】 Er:YAGレーザーによるSRPをハンドスケーラーと比較して同等の経過が得られた一症例を示す9)。この患者は全顎的な知覚過敏を主訴に来院し、中等度の歯周ポケットが認められた(図4)。倫理委員会の承認のもと臨床研究として、下顎右側、左側をそれぞれレーザー治療(図5)、ハンドスケーリングとして治療を行った(図6)。
その結果、処理時間はレーザー側の方が要したが、術中の不快感はレーザー処置の方で低く、術後の経過は両群とも良好で、同等の歯周ポケットの回復を示すことができ(図7)、安定した状態でメインテナンスへ移行している。
近年は、いくつかのメタ解析(図8)によりSRPよりもEr:YAGレーザー治療の方が僅かではあるが、有意のポケットの減少やアタッチメントゲインがあること10)や、システマティックレビューでは統計学的に有意差がなくとも個々の報告からは有用性が認められ得るという報告がなされている11)。
2015年に米国歯科医学会はSRPへの併用療法の意義についてシステマティックレビュー12)、およびそれに基づくガイドラインでレーザーについて「7mm以上の歯周ポケットへのEr系レーザーならびにNd:YAGレーザーの併用療法は従来法単独を上回る」としており、2018年のアメリカ歯周病学会の声明13)においてもその表現は引用されている。
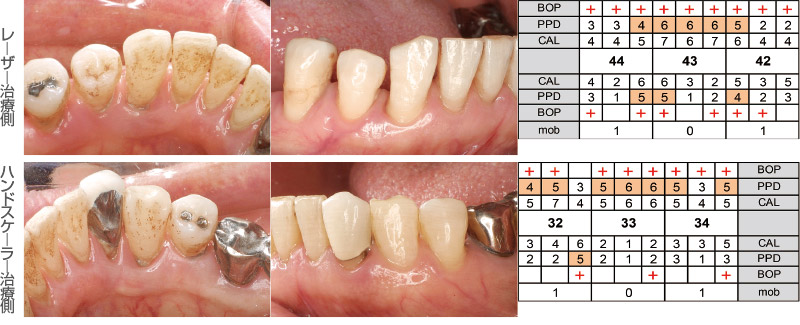
図4 広汎型中等度慢性歯周炎の62歳男性、SRP前の状態。上はEr:YAGレーザー単独で、下はハンドスケーラーでSRPを行う(文献9より改編)。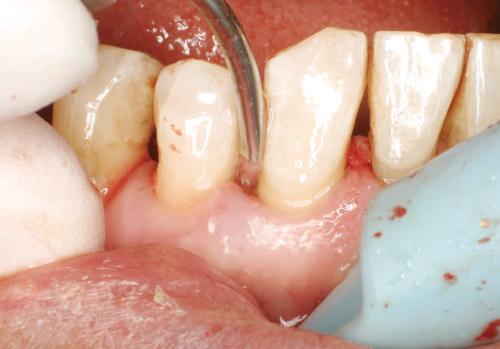
図5 局所麻酔後に20PPS、60mJ、注水下で歯肉縁下のデブライドメント。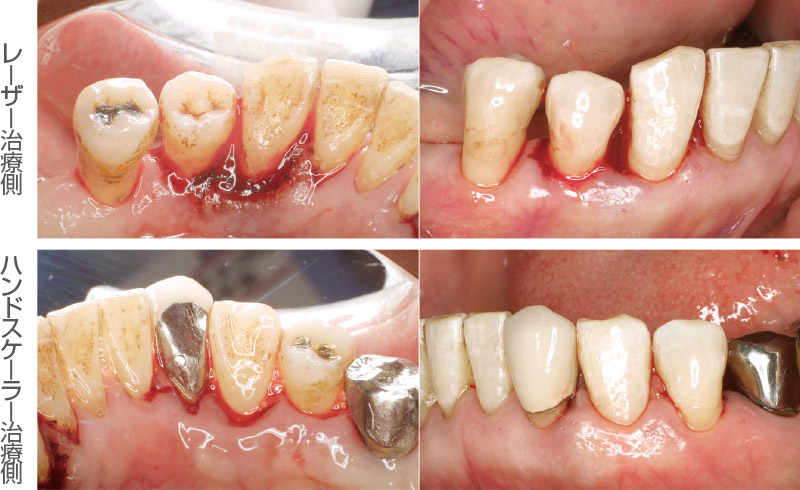
図6 術直後(上はEr:YAGレーザー、下はハンドスケーラー)。術中の不快感はレーザー治療のほうが少なかった。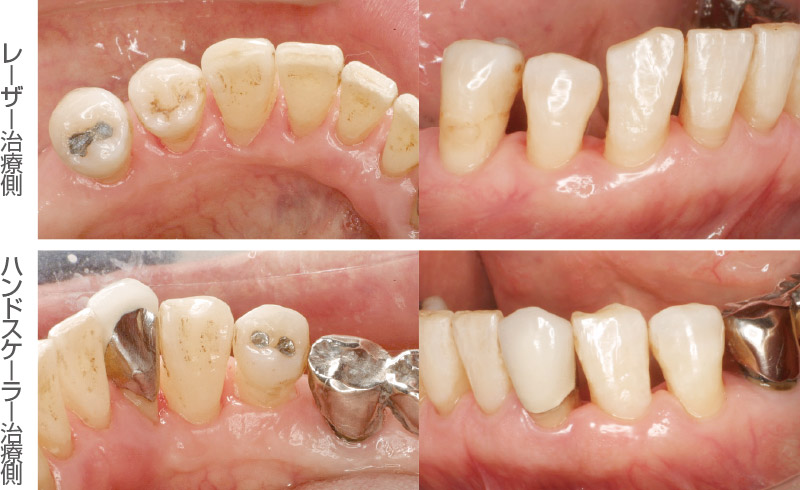
図7 術後3ヵ月。共に歯周ポケットは3mm以下となり、その後のメインテナンスでも良好な状態を維持できている。
図8 Er:YAGレーザーの非外科的歯周治療に関する近年の主なシステマティックレビュー(文献15より改編)
■3. 新しい非外科的術式「Er-LCPT」
非外科的な歯周治療の成績を向上させるために、Aokiらは従来のSRPにEr:YAGレーザーを、ダイナミックに併用した新規のEr:YAG Laser-assisted Comprehensive Periodontal Pocket Therapy(Er-LCPT)14、15)を開発した(図9)。
SRPと併せて、根面へのレーザー照射により殺菌無毒化を徹底し、ポケット軟組織壁内面の深行上皮や炎症性結合組織の除去を行い、骨欠損の掻爬も確実に行う。レーザーによる欠損部のデブライドメントは出血を生じるが、これは血餅として術後の治癒につながるため16)止血はあえては行わない。また、ポケット内で照射をすることで周囲の組織へ低出力のエネルギーが浸透し、細胞レベルでの活性化を期待している。また、ポケット周囲の外側の上皮の除去により、術後のポケット内への上皮のダウングロースを遅延させる効果を狙っている。
最後は、ポケット入り口部分で非接触照射をすることで、血液の表面を凝固させて血餅の保持を促進し治癒の促進を図る。
【症例2】 66歳男性、歯周基本治療後に右上側切歯の近心に深い垂直性欠損が残存しプロービングポケット深さは8mmを示したため、Er-LCPTを行った。20Hz、80mJで前述の処置を行い、術直後の出血は血餅の表面を凝固させて欠損内に安定化させた(図10a、b)。
術後3ヵ月では歯肉の陥凹が見られるが、ポケットは2mmに減少し、1年後には歯肉の形態も改善した(図10c、d)。X線検査では術前に見られた骨欠損が、歯根膜腔を伴ってほぼ回復していることが観察された(図11)15)。
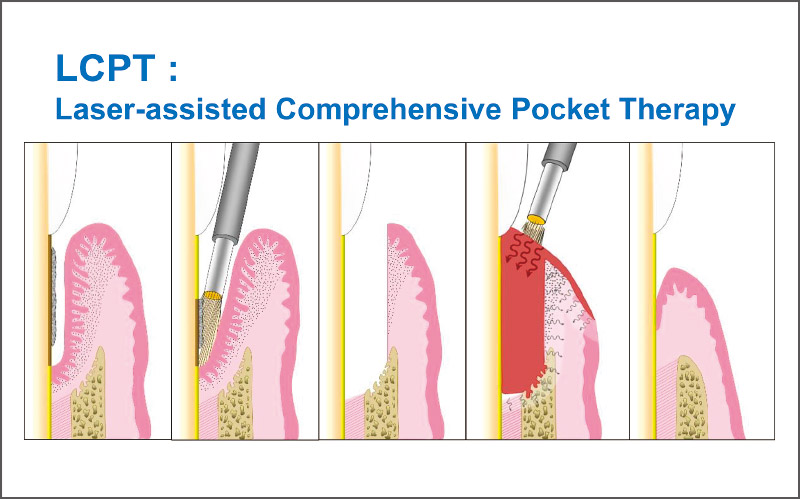
図9 Er-LCPTでは根面デブライドメントだけでなく、ポケット内の肉芽組織の掻爬もレーザーで行う。出血への非接触照射により血餅の安定を図る(文献14より改編)。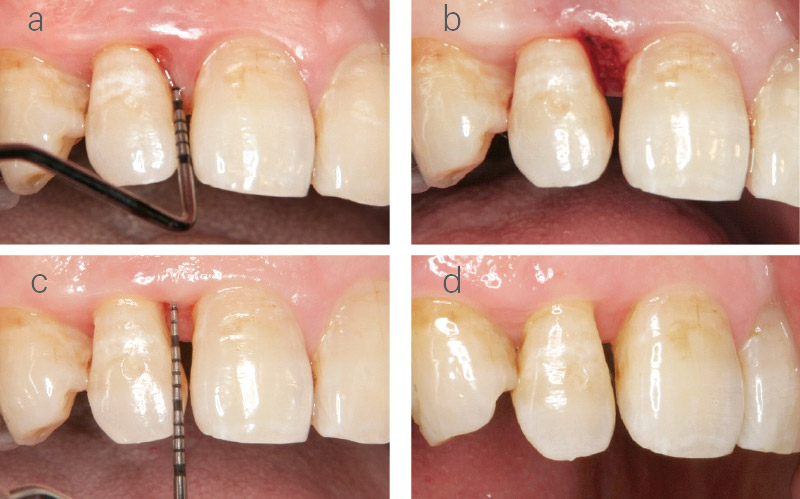
図10 2近心に8mmのポケットがみられ(a)、Er-LCPTを行った(b)。術後3ヵ月でポケットは2mm(c)、1年で歯肉形態も回復(d)。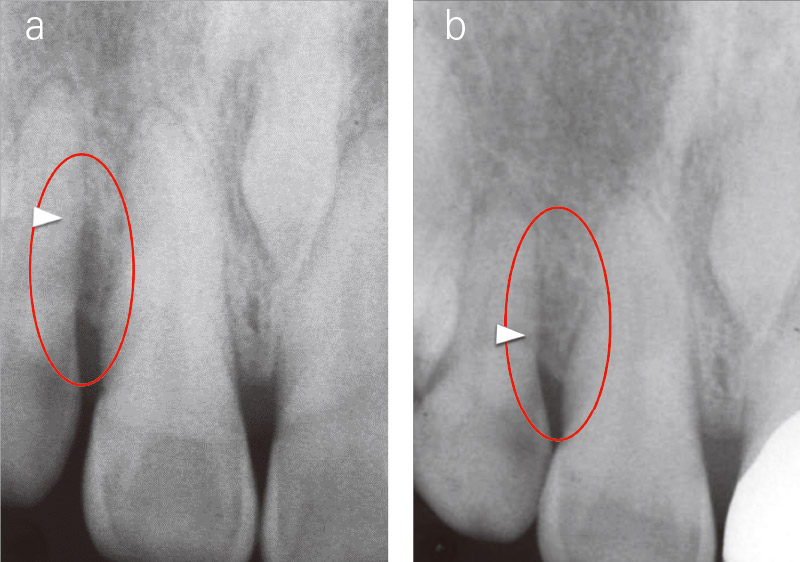
図11 X線画像にて術前は深い垂直性欠損(a)。術後1年では改善がみられた(b)。(文献15より改編)
■4. 低侵襲の歯周外科への応用―マイクロサージェリーとのコンビネーション―
Erwin Adverl EVOの特徴として、様々な部位にアプローチできる細いコンタクトチップが挙げられる。チップ先端と同軸の注水が正確になされ、硬組織と軟組織の両者に繊細な処置が可能である。この特徴は、歯科用顕微鏡との治療に非常に相性が良い。処置部位を限局的にし、正確に組織蒸散を熱傷害なく実現できるこの組み合わせは、まさにMinimally invasive(MI)のコンセプトに合致する診療アプローチと考えられる15)。
歯肉の審美治療への応用例として、メラニン色素の除去とメタルタトゥー除去が挙げられる。いずれも顕微鏡下で行うことで、原因となっているメラノサイトを含んだ上皮層(図12、13)や結合組織に埋入した金属切削片(図14、15)を正確に、低侵襲に除去できる。その結果、痛みが少なく、再発しにくい治療が可能で、患者の満足度が高い。
また、フラップ手術では、Er:YAGレーザーレーザーの細いチップは、根分岐部病変や垂直性骨欠損のデブライドメントに適しており、動物実験16)および臨床応用で従来法よりも優れた治癒を示す18)ことが報告されている。一方、近年の歯周外科治療においては、MIでの外科手技の有効性が報告されており19)、筆者らはEr-LCPTのアプローチと組み合わせることで良好な経過を示した症例を経験している。
【症例3】【 患者は82歳女性。年齢、全身状態(高血圧、骨粗鬆症)を考慮し、9mmのポケットから排膿している右側切歯(図16)の頰側歯肉のみを剥離するsingle flap approachにて、明視野下でのデブライドメントをEr:YAGレーザーにて行った(図17)。
2壁性骨欠損であり(図18)、血餅として保持を促すようなディフォーカス照射17)を行った(図19)。最小の切開で弁の安定性を確保した部位に、血餅の保持をより確実に行うことで、再生材料を使用せずに優れた治癒を得ることができた(図20、21)。
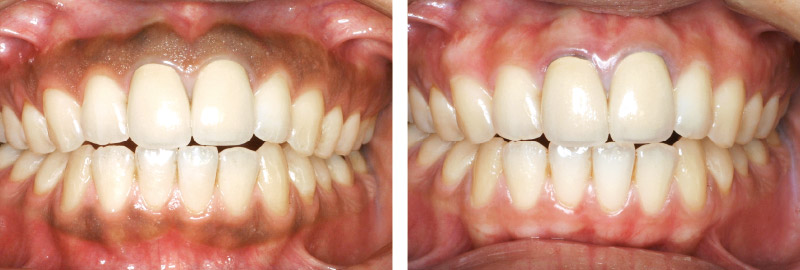
図12 全顎的にEr:YAGレーザー(注水、20Hz、80mJ)で歯肉のメラニン除去を行った症例の術前(左)と術後6ヵ月(右)。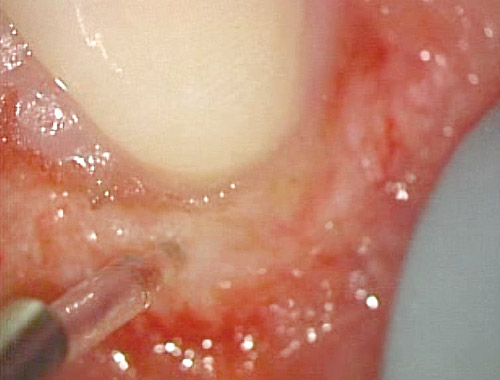
図13 術中の顕微鏡画像。顕微鏡によりメラニン沈着部位を確認することで侵襲を最小にし、かつ再発を防止できる。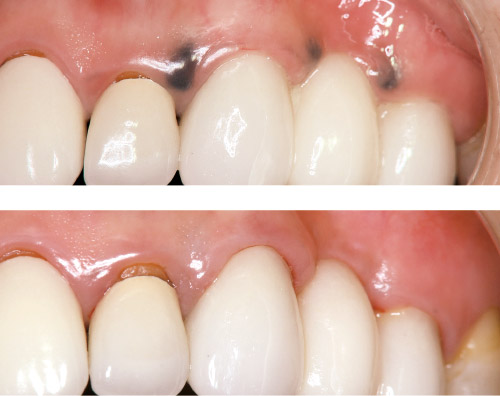
図14 2~5のメタルタトゥー除去をEr:YAGレーザー(注水、10Hz、60mJ)で行った術前(上)と術後6ヵ月(下)。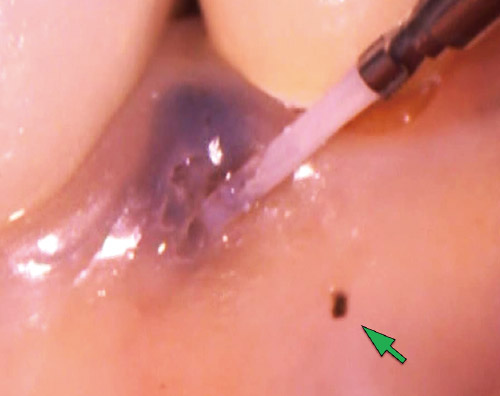
図15 術中の顕微鏡画像。原因である金属切削片(矢印)の徹底的な除去には顕微鏡は不可欠である。歯肉蒸散量を最小にして歯肉退縮を防ぐ。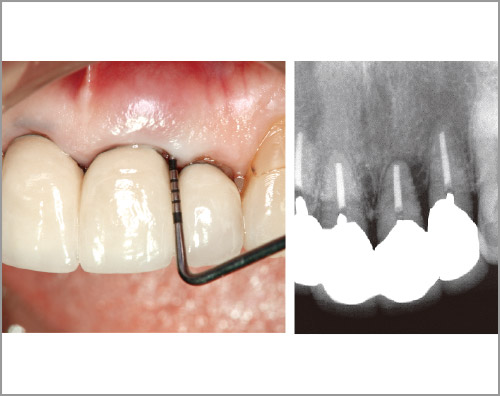
図16 82歳の女性。術前に 1遠心に9mmの歯周ポケットがみられ、排膿を示した。X線画像にて根尖付近におよぶ骨欠損を認めた。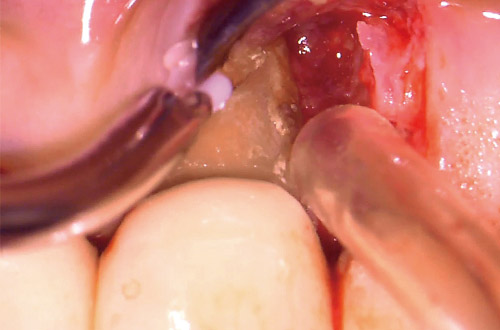
図17 single flap approachにより頰側歯肉のみ剥離し、マイクロサージェリーでEr:YAGレーザーによる歯石除去(注水、20Hz、80mJ)。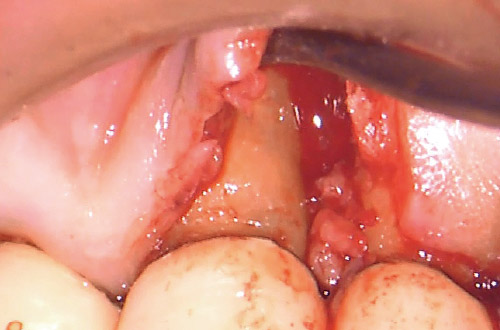
図18 デブライドメント後。Er:YAGレーザー照射後の骨面からは出血が多い。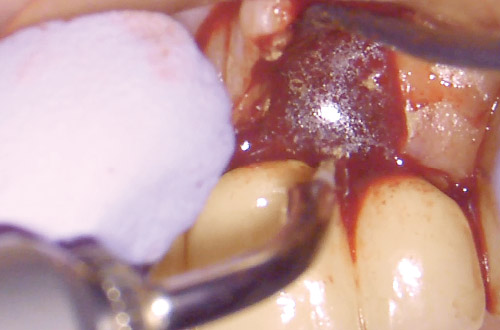
図19 ディフォーカス照射。血餅表面を非注水のディフォーカス照射により凝固させ、血餅の骨欠損内での安定化を図り、その後に弁を復位縫合。再生療法の材料は用いていない。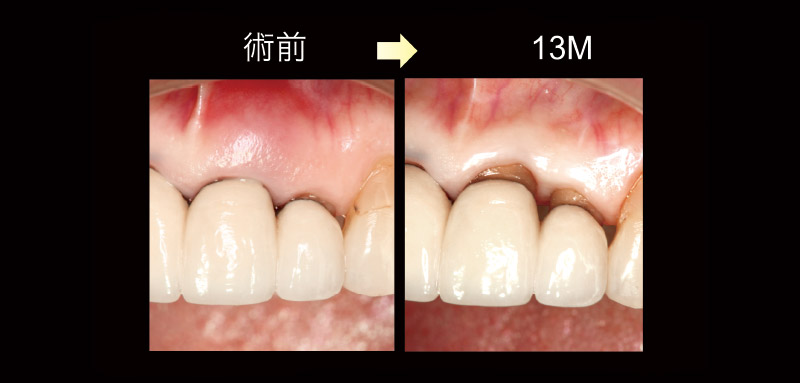
図20 術前と術後の変化。術後13ヵ月でポケット深さは2mmとなり、6mmのクリニカルアタッチメントゲインを示した。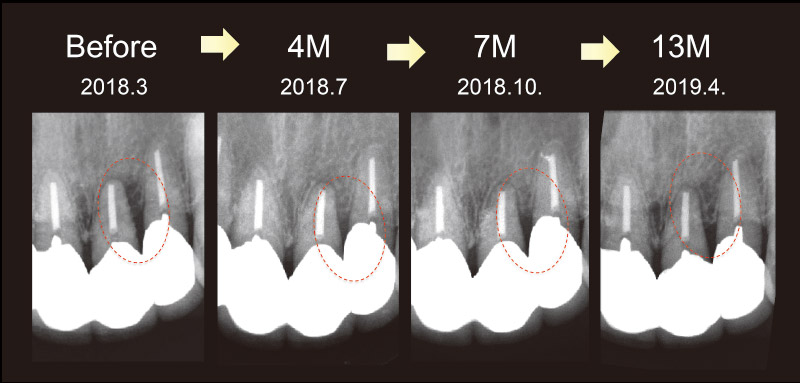
図21 術後のX線画像の変化。術後4ヵ月にて骨欠損のある程度の不透過性が亢進し、7ヵ月に歯根膜腔の回復、13ヵ月で明瞭な歯槽硬線を伴う骨組織が観察された。
■5. 治癒と組織再生を促進するメカニズム
歯周組織の創の閉鎖や組織の治癒において重要な要素として、血餅の安定、根面への細胞の遊走と付着、細胞の増殖と分化が挙げられる。レーザー照射根面や切削骨面20)は血餅が付着しやすく、ディフォーカス照射で血餅表面を凝固させると極めて安定度が増す17)。また、レーザー照射根面はスメア層が無く、細胞の遊走や付着に有利21)と考えられている。
さらに、近年明らかになりつつあるレーザーの低出力のエネルギーによる生体刺激効果として、歯肉線維芽細胞22)、骨芽細胞23)など歯周組織に関わる細胞で細胞増殖効果が確認されている。これらの効果が複合的に作用して治癒、ひいては再生効果の促進へとつながると考えられる(図22)。
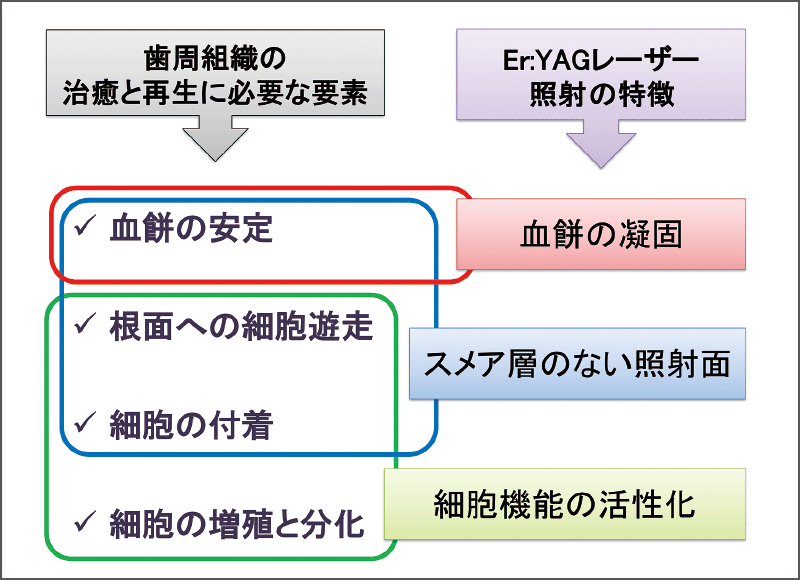
図22 歯周組織の治癒・再生に必要な要素の観点から、Er:YAGレーザー照射後の歯根面の特徴は利点が多い。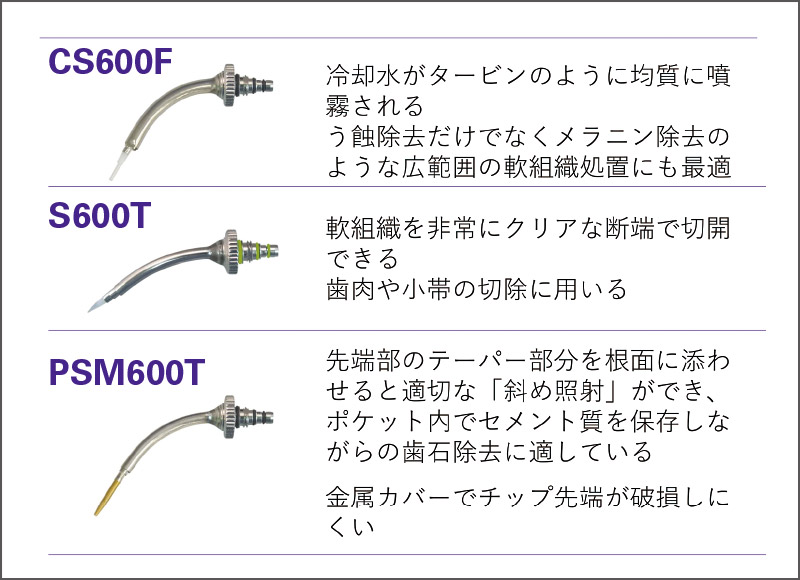
図23 歯周治療で使いやすいErwin Adverl EVOのコンタクトチップ
■まとめ
「なぜEr:YAGレーザー治療は歯周治療で効果があるのか?」という問いに、現段階ではレーザーで包括的に原因除去をし、さらに治癒を促す複数の因子が互いに影響した結果であると答えることができる。特にEr-LCPTやEr-LBRT(本誌14ページの谷口論文参照)などで用いる非注水で血餅の表面を凝固させて安定を促進するテクニックは、Er:YAGレーザーの効果をこれまで以上に引き出し、従来の歯周治療とは異なる新しい側面を有することで効果を倍加させている。
Erwin Adverl EVOは実際の臨床で使いやすいチップが多くそろっており、各自の臨床のスタイルにマッチするチップを適切に選択する(図23)と、症例にあったMIな治療が可能となる。
今後もさらに有効な歯周光線治療の発展と使いやすいチップの開発のための基礎研究や臨床研究をErwin AdverlEVOが牽引していくことが期待される。
- 1) Aoki, A., et al. In vitro studies on laser scaling of subgingival calculus with an erbium:YAG laser. J. Periodontol. 65, 1097-1106 (1994).
- 2) Aoki, A., et al. In vitro evaluation of Er:YAG laser scaling of subgingival calculus in comparison with ultrasonic scaling. J. Periodontal Res. 35, 266-277 (2000).
- 3) Lin, T., et al. Energy output reduction and surface alteration of quartz tips following Er:YAG laser contact irradiation on soft and hard tissues in vitro. Dent. Mater. J. 35, 51-62 (2016).
- 4) 青木章ら. ポジション・ペーパー(学会見解論文)レーザーによる歯石除去 監修:特定非営利活動法人日本歯周病学会,日本レーザー歯学会. 日本歯周病学会会誌 52, 180-190 (2010).
- 5) Ando,Y., et al. Bactericidal effect of erbium YAG laser on periodontopathic bacteria. Lasers Surg Med 19, 190-200 (1996).
- 6) Akiyama, F., et al. In vitro studies of the ablation mechanism of periodontopathic bacteria and decontamination effect on periodontally diseased root surfaces by erbium:yttrium-aluminum-garnet laser. Lasers Med. Sci. 26, 193-204 (2011).
- 7) Yamaguchi, H., et al. Effects of irradiation of an erbium:YAG laser on root surfaces. J Periodontol 68, 1151-1155 (1997).
- 8) Schwarz, F., et al. Periodontal treatment with an Er:YAG laser or scaling and root planing. A 2-year follow-up split-mouth study. J Periodontol 74, 590-596 (2003).
- 9) Ishikawa, I., et al. Application of lasers in periodontics: true innovation or myth? Periodontol. 2000 50, 90-126 (2009).
- 10) Sgolastra, F., et al. Efficacy of Er:YAG laser in the treatment of chronic periodontitis: systematic review and meta-analysis. Lasers Med. Sci. 27, 661-673 (2012).
- 11) Zhao, Y., et al. Er:YAG laser versus scaling and root planing as alternative or adjuvant for chronic periodontitis treatment: a systematic review. J. Clin. Periodontol. 41, 1069-1079 (2014).
- 12) Smiley, C.J., et al. Systematic review and meta-analysis on the nonsurgical treatment of chronic periodontitis by means of scaling and root planing with or without adjuncts. J. Am. Dent. Assoc. 146, 508-524 e505 (2015).
- 13) Mills, M.P., et al. American Academy of Periodontology best evidence consensus statement on the efficacy of laser therapy used alone or as an adjunct to non-surgical and surgical treatment of periodontitis and peri-implant diseases. J. Periodontol. 89, 737-742 (2018).
- 14) Aoki, A., et al. Periodontal and peri-implant wound healing following laser therapy. Periodontol. 2000 68, 217-269 (2015).
- 15) Mizutani, K., et al. Lasers in minimally invasive periodontal and peri-implant therapy. Periodontol. 2000 71, 185-212 (2016).
- 16) Mizutani, K., et al. Periodontal tissue healing following flap surgery using an Er:YAG laser in dogs. Lasers Surg. Med. 38, 314-324 (2006).
- 17) Taniguchi, Y., et al. A Novel Surgical Procedure for Er:YAG Laser-Assisted Periodontal Regenerative Therapy: Case Series. Int. J. Periodontics Restorative Dent. 36, 507-515 (2016).
- 18) Gaspirc, B. & Skaleric, U. Clinical evaluation of periodontal surgical treatment with an Er:YAG laser: 5-year results. J. Periodontol. 78, 1864-1871 (2007).
- 19) Liu, S., et al. Minimally Invasive Surgery Combined with Regenerative Biomaterials in Treating Intra-Bony Defects: A Meta-Analysis. PLoS One 11, e0147001 (2016).
- 20) Ohsugi, Y., et al. Evaluation of bone healing following Er:YAG laser ablation in rat calvaria compared with bur drilling. J Biophotonics, e201800245 (2018).
- 21) Maruyama, H., et al. The effect of chemical and/or mechanical conditioning on the Er:YAG laser-treated root cementum: analysis of surface morphology and periodontal ligament fibroblast attachment. Lasers Surg. Med. 40, 211-222 (2008).
- 22) Kong,S., et al.Biological effects of Er:YAG laser irradiation on the proliferation of primary human gingival fibroblasts. J Biophotonics 11(2018).
- 23) Aleksic, V., et al. Low-level Er:YAG laser irradiation enhances osteoblast proliferation through activation of MAPK/ERK.Lasers Med. Sci. 25, 559-569 (2010).
同じ筆者の記事を探す【 青木 章 】
モリタ友の会会員限定記事
同じテーマの記事を探す【 レーザー 】
モリタ友の会会員限定記事
- 179号 Clinical Report 歯周病患者におけるEr:YAGレーザーの日常臨床への導入 SPTを通じた歯科衛生士との連携
- 178号 Clinical Report 歯周病治療におけるEr:YAGレーザーの臨床的有用性
- 177号 Clinical Report Erwin AdvErL EVOの臨床応用の有用性と実際
- 176号 Clinical Report 日常臨床におけるEr: YAGレーザー
- 175号 Clinical Report Erwin AdvErL EVO を使用した口腔軟組織の切開、切除の実際
目 次
モリタ友の会会員限定記事
- Trends 歯周検査がPam で変わる!『歯周ポケット測定器「Pam」』について
- Clinical Report 「Veraview X800」を使った副鼻腔の読影法と経歯槽頂上顎洞挙上手術における活用法
- Clinical Report 臼歯部2級窩洞コンポジットレジン充填修復のコツ~セクショナルマトリックスシステムを用いた隣接面へのアプローチ~
- Trends 「スーパーMTA ペースト」−MTAとTBBが協奏する新しいMTA系材料−
- Interview 腎臓内科医から見た医科歯科連携−歯科医師が知っておくべき睡眠時無呼吸症候群(SAS)の見分け方−
- Clinical Report 歯周ポケット測定器「Pam」と モリタDOOR システムの 連携について
- Field Report 埋入ステップがシンプル 初心者にも扱いやすいインプラントシステム
- Clinical Report 歯周治療に「Erwin Adverl EVO」を 徹底活用する ―エビデンスに基づいたEr:YAG レーザーの炎症コントロールと治癒促進―
- Field Report 音波水流が魅力の音波式電動歯ブラシで歯周病再発防止へ
- Demo Report 臼歯までしっかりフィット!磨いた後のツルツル感が違います
- Demo Report 豊富なラインアップを実感。 提案の幅が広がりそうです
- Technical Report 歯科用陶材「セラビアンZR FC ペーストステイン」の有効な使用方法
- Field Report PMTC後のキレイな状態を維持する セルフケアに適した音波式電動歯ブラシ
他の記事を探す
モリタ友の会
セミナー情報
会員登録した方のみ、
限定コンテンツ・サービスが無料で利用可能
オンラインカタログでの製品の価格チェックやすべての記事の閲覧、臨床や経営に役立つメールマガジンを受け取ることができます。
商品のモニター参加や、新製品・優良品のご提供、セミナー優待割引のある、もっとお得な有料会員サービスもあります。






























